อะตอมเเละสมบัติของธาตุ
อะตอมประกอบด้วยอนุภาคที่มีขนาดเล็กมากเเละไม่สามารถมองเห็นได้ด้วยตาเปล่า ซึ่งเเนวคิดนี้ได้เริ่มขึ้นในสมัยกรีกโบราณ โดยดิโมคริตุส คำว่า อะตอม (atom) ซึ่งมาจากคำในภาษากรีก ซึ่งเเปลว่า "เเบ่งเเยกอีกไม่ได้"
2.1 เเบบจำลองอะตอม
อะตอมมีขนาดเล็กมากและมองไม่เห็นด้วยตาเปล่า แบบจำลองอะตอมมีวิวัฒนาการดังนี้
2.1.1 แบบจำลองอะตอมของจอร์น ดอลตัน
ในปี พ.ศ. 2346 (ค.ศ. 1803) จอห์น ดอลตัน (John Dalton) นักวิทยาศาสตร์ชาวอังกฤษได้เสนอทฤษฎีอะตอมเพื่อใช้อธิบายเกี่ยวกับการเปลี่ยนแปลงของสารก่อนและหลังทำปฏิกิริยา รวมทั้งอัตราส่วนโดยมวลของธาตุที่รวมกันเป็นสารประกอบ ซึ่งสรุปได้ดังนี้
1. ธาตุประกอบด้วยอนุภาคเล็ก ๆ อนุภาคเหล่านี้เรียกว่า อะตอม ซึ่งแบ่งแยกและทำให้
สูญหายไม่ได้
2. อะตอมของธาตุชนิดเดียวกันมีสมบัติเหมือนกัน เช่น มีมวลเท่ากัน แต่จะมีสมบัติแตกต่าง
จากอะตอมของธาตุอื่น
3. สารประกอบเกิดจากอะตอมของธาตุมากกว่าหนึ่งชนิดทำปฏิกิริยาเคมีกันในอัตราส่วนที่เป็น
เลขลงตัวน้อย ๆ
แบบจำลองอะตอมตามทฤษฎีของดอลตัน
ทฤษฎีอะตอมของดอลตันช่วยให้นักวิทยาศาสตร์ในสมัยนั้นสามารถอธิบายลักษณะและสมบัติของอะตอมได้เพียงระดับหนึ่ง ต่อมาได้มีการศึกษาเกี่ยวกับอะตอมเพิ่มขึ้น และค้นพบว่ามีข้อมูลบางประการไม่สอดคล้องกับแนวคิดของดอลตัน เช่น พบว่าอะตอมของธาตุชนิดเดียวกันมีมวลแตกต่างกันได้ อะตอมสามารถแบ่งแยกได้ แนวคิดเกี่ยวกับทฤษฎีอะตอมของดอลตันจึงไม่ถูกต้อง
2.1.2 แบบจำลองอะตอมของทอมสัน
นักวิทยาศาสตร์หลายคนได้ศึกษาการนำไฟฟ้าของแก๊ส โดยทดลองเกี่ยวกับผลของการใช้
ความต่างศักย์ไฟฟ้าสูงต่อการเคลื่อนที่ของประจุไฟฟ้าของอะตอมแก๊ส เพื่อให้ได้ข้อมูลที่ให้รายละเอียดเกี่ยวกับโครงสร้างภายในอะตอม โดยการผ่านไฟฟ้ากระแสตรงเข้าไปในหลอดแก้วบรรจุแก๊สความดันต่ำ (ดูดอากาศออก) ซึ่งที่ภาวะนี้มีจำนวนอะตอมของแก๊สไม่หนาแน่น ประจุไฟฟ้าสามารถเดินทางได้ไกลและพบว่าเมื่อเพิ่มความต่างศักย์ระหว่างขั้วไฟฟ้าให้สูงขึ้นจะมีกระแสไฟฟ้าไหลผ่านตลอด ขณะเดียวกันจะมีรังสีออกจากแคโทดไปยังแอโนด รังสีนี้เรียกว่า รังสีแคโทด (cathode ray) เรียกหลอดแก้วชนิดนี้ว่า หลอดรังสีแคโทด (cathode ray tube) เนื่องจากมนุษย์ไม่สามารถมองเห็นรังสีแคโทดด้วยตาเปล่าได้ ดังนั้น เพื่อให้สามารถติดตามทิศทางการเคลื่อนที่ของรังสีแคโทดได้ จึงต้องฉาบสารเรืองแสง เช่น ซิงค์ซัลไฟด์ ฟอสฟอรัส ไว้ที่ฉาก เมื่อรังสีแคโทดตกกระทบที่ฉากจะปรากฏเป็นจุดเรืองแสงที่สามารถสังเกตเห็นด้วยตาเปล่าได้
นักวิทยาศาสตร์ได้ทำการทดลองเพื่อศึกษาการเคลื่อนที่ของรังสีแคโทดโดยให้เคลื่อนที่ผ่าน
สนามไฟฟ้าดังรูป 2.2 ก) พบว่าแนวการเคลื่อนที่เบนไปจากเดิม โดยเบนเข้าหาขั้วบวกของสนามไฟฟ้า
เนื่องจากรังสีแคโทดเบนเข้าหาขั้วบวกของสนามไฟฟ้าจึงสรุปว่ารังสีแคโทดประกอบด้วยอนุภาคที่มี
ประจุไฟฟ้าลบ เมื่อศึกษาเพิ่มเติมโดยให้รังสีแคโทดเคลื่อนที่ผ่านสนามแม่เหล็กดังรูป 2.2 ข) พบว่า
แนวการเคลื่อนที่เบนไปจากเดิมเช่นกัน

ในช่วงปี พ.ศ. 2440 โจเซฟ จอห์น ทอมสัน (Joseph John Thomson) นักวิทยาศาสตร์ชาวอังกฤษ
ทำการทดลองโดยให้รังสีแคโทดเคลื่อนที่ผ่านสนามไฟฟ้าที่ตั้งฉากกับสนามแม่เหล็ก และปรับขนาด
ของสนามไฟฟ้าให้พอเหมาะจนกระทั่งทิศทางการเคลื่อนที่ของรังสีแคโทดไม่เบนไปจากแนวเดิม ดังรูป
2.2 ค) ซึ่งสภาวะนี้แรงที่เกิดขึ้นจากสนามไฟฟ้าและสนามแม่เหล็กมีขนาดเท่ากันแต่มีทิศตรงข้ามกัน
จากข้อมูลการทดลองร่วมกับทฤษฎีทางแม่เหล็กไฟฟ้าทำให้ทอมสันนำมาใช้คำนวณอัตราส่วนของ
ประจุต่อมวล (e/m) ของรังสีแคโทดได้ ทอมสันได้ทดลองเพื่อศึกษาอัตราส่วนของประจุต่อมวล
ของรังสีแคโทดซ้ำหลายครั้งโดยเปลี่ยนชนิดของแก๊สและชนิดของโลหะที่ใช้ทำขั้ว แคโทดปรากฏว่า
อัตราส่วนของประจุต่อมวลของรังสีแคโทดมีค่าโดยประมาณเท่ากันคือ 1.76 × 10⁸ คูลอมบ์ต่อกรัม
(C/g) จึงสรุปว่าอนุภาครังสีแคโทดที่ออกมาจากโลหะต่างชนิดเป็นอนุภาคชนิดเดียวกัน ซึ่งต่อมาได้
เรียกอนุภาคนี้ว่า อิเล็กตรอน (electron)
การค้นพบอิเล็กตรอนทำให้ทอมสันสรุปได้ว่า อะตอมทุกชนิดมีอิเล็กตรอนเป็นองค์ประกอบ ซึ่งลบล้างแนวคิดที่ว่าอะตอมแบ่งแยกไม่ได้ และเนื่องจากสารต่าง ๆ ที่อยู่ในสภาวะปกติจะเป็นกลางทางไฟฟ้า นักวิทยาศาสตร์จึงสรุปว่า อะตอมเป็นกลางทางไฟฟ้า ซึ่งจากข้อมูลดังกล่าวทำให้ทอมสันเสนอแบบจำลองของอะตอมว่า อะตอมเป็นรูปทรงกลมประกอบด้วยเนื้ออะตอมซึ่งมีประจุบวกและอิเล็กตรอนซึ่งมีประจุลบกระจายอยู่ทั่วไป ดังรูป 2.3 อะตอมในสภาพที่เป็นกลางทางไฟฟ้าจะมีจำนวนประจุบวกเท่ากับจำนวนประจุลบ

ทอมสันเป็นนักวิทยาศาสตร์คนแรกที่เสนอรายละเอียดภายในอะตอม ทำให้มโนภาพของอะตอมชัดเจนขึ้น อย่างไรก็ตามในช่วงเวลาต่อมานักวิทยาศาสตร์ได้ทำการทดลองเพิ่มเติมและมีข้อมูลเพิ่มขึ้น ซึ่งแบบจำลองอะตอมของทอมสันไม่สามารถอธิบายได้
2.1.3 แบบจำลองอะตอมของรัทเทอร์ฟอร์ด
เมื่อปี พ.ศ. 2454 เออร์เนสต์ รัทเทอร์ฟอร์ด (Ernest Rutherford) นักวิทยาศาสตร์ชาวอังกฤษ
และ ฮันส์ ไกเกอร์ (Hans Geiger) นักวิทยาศาสตร์ชาวเยอรมัน ได้พิสูจน์แบบจำลองอะตอมของ
ทอมสันโดยการยิงอนุภาคแอลฟาไปยังแผ่นทองคำบาง ๆ
รัทเทอร์ฟอร์ดอธิบายลักษณะภายในอะตอมว่า การที่รังสีแอลฟาส่วนใหญผ่านแผ่น ทองคำ ไปได้
แสดงว่า ภายในอะตอมต้องมีที่ว่างอยู่เป็นบริเวณกว้าง การที่รังสีแอลฟาบางอนุภาคเบี่ยงเบนหรือสะท้อนกลับมาบริเวณด้านหน้าของฉากเรืองแสง แสดงว่าภายในอะตอมน่าจะมีกลุ่มอนุภาคที่มีขนาดเล็กมาก มีมวลสูงมากกว่ารังสีแอลฟาและมีประจุบวก รัทเทอร์ฟอร์ดจึงได้เสนอแบบจำลองอะตอมใหม่ว่า อะตอมประกอบด้วยนิวเคลียสที่มีขนาดเล็กมากอยู่ภายในและมีประจุไฟฟ้าเป็นบวก โดยมีอิเล็กตรอนเคลื่อนที่อยู่รอบ ๆ ดังรูป 2.4

ตามแบบจำลองของรัทเทอร์ฟอร์ด ภายในอะตอมมีนิวเคลียสซึ่งมีขนาดเล็กมาก เมื่อเทียบกับ
ขนาดของอะตอม รังสีแอลฟาจึงมีโอกาสชนนิวเคลียสได้น้อยมาก ส่วนอิเล็กตรอนที่อยู่รอบนิวเคลียส
มีมวลน้อยมาก การชนกับอิเล็กตรอนจึงไม่มีผลทำให้ทิศทางการเคลื่อนที่ของรังสีแอลฟาเปลี่ยนไป
รังสีส่วนใหญ่จึงทะลุแผ่นทองคำไปเป็นแนวตรง มีบางครั้งที่รังสีแอลฟาวิ่งเฉียดนิวเคลียส ซึ่งจะถูก
ประจุของนิวเคลียสผลักให้เบนไปจากแนวเส้นตรง ส่วนรังสีแอลฟาที่วิ่งตรงไปยังนิวเคลียสซึ่งมีมวล
มากก็จะถูกผลักให้สะท้อนกลับ ดังแสดงในรูป 2.5
รูป 2.5 การใช้แบบจำลองอธิบายผลการทดลองของรัทเทอร์ฟอร์ด
ตามแนวคิดของรัทเทอร์ฟอร์ดจะพบว่ามวลส่วนใหญ่ของอะตอมคือมวลของนิวเคลียส ส่วน
อิเล็กตรอนถึงแม้จะเป็นส่วนประกอบที่ทำให้อะตอมมีขนาดใหญ่แต่มีมวลน้อยมากจนถือว่าไม่มีผล
ต่อมวลของอะตอม
แบบจำลองอะตอมของรัทเทอร์ฟอร์ด ไม่ได้อธิบายว่าอิเล็กตรอนอยู่รอบนิวเคลียสในลักษณะใด
นักวิทยาศาสตร์จึง ได้ทำการทดลองเพื่อ รวบรวมข้อมลูเพิ่มเติมเกี่ยวกับตำแหน่งของอิเล็กตรอนเพื่อ นำ
มาสร้างเป็นแบบจำลองที่มีความสมบูรณ์มากยิ่งขึ้น
2.1.4. แบบจำลองอะตอมของโบร์
สเปกตรัมแม่เหล็กไฟฟ้าประกอบด้วยคลื่นแม่เหล็กไฟฟ้าที่มีความยาวคลื่นต่าง ๆ กัน และมี
ความถี่ต่อเนื่องกันเป็นช่วงกว้าง มีทั้งที่มองเห็นได้และมองไม่เห็น มีชื่อเรียกต่าง ๆ กัน แสงที่ประสาท
ตาของมนุษย์สามารถรับรู้ได้เรียกว่า แสงที่มองเห็นได้ (visible light) มีความยาวคลื่นอยู่ในช่วง
400–700 นาโนเมตร ซึ่งประกอบด้วยแสงสีต่าง ๆ กัน แต่ประสาทตาของมนุษย์ไม่สามารถแยกแสง
ที่มองเห็นเป็นสีต่าง ๆ ได้เอง ทำให้มองเห็นสีรวมกัน ซึ่งเรียกว่า แสงขาว (white light) และเมื่อให้
แสงขาวส่องผ่านปริซึม แสงขาวจะแยกออกเป็นแสงสีรุ้งต่อเนื่องกัน เรียกว่า แถบสเปกตรัมของแสง
ขาว ดังรูป 2.6
มักซ์ พลังค์ (Max Planck) นักวิทยาศาสตร์ชาวเยอรมัน ได้ศึกษาพลังงานของคลื่นแม่เหล็กไฟฟ้าและได้ข้อสรุปเกี่ยวกับความสัมพันธ์ระหว่างพลังงานของคลื่นแม่เหล็กไฟฟ้ากับความถี่ของคลื่นนั้นว่า พลังงานของคลื่นแม่เหล็กไฟฟ้าแปรผันตามความถี่ของคลื่นและแปรผกผันกับความยาวคลื่น ดังความ สัมพันธ์ต่อไปนี้
เมื่อ E คือพลังงานของคลื่นแม่เหล็กไฟฟ้า มีหน่วยเป็น จูล h คือค่าคงตัวของพลังค์ มีค่า 6.626 × 10^-34 จูลวินาที ν คือความถี่ของคลื่นแม่เหล็กไฟฟ้า มีหน่วยเป็นเฮิรตซ์ c คือความเร็วของคลื่นแม่เหล็กไฟฟ้าในสุญญากาศ ซึ่งเท่ากับ 2.997 × 10^8 เมตรต่อวินาที(อาจใช้3.0 × 10^8 เมตรต่อวินาที)
และ λ คือความยาวคลื่นของคลื่นแม่เหล็กไฟฟ้า หน่วยเป็นเมตร
ความสัมพันธ์ดังกล่าวนี้เมื่อนำ มาคำ นวณพลังงานของแถบสีต่าง ๆ ในสเปกตรัมของแสงขาว ซึ่งมีความยาวคลื่นต่าง ๆ จะได้ดังนี้
สเปกตรัมจากแสงอาทิตย์มีแสงสีต่อเนื่องกันเป็น แถบสเปกตรัม (spectrum band) ส่วนสเปกตรัมที่มองเห็นจากหลอดฟลูออเรสเซนต์นอกจากจะมองเห็นแถบสเปกตรัม ของสีต่าง ๆ เป็นพื้นแล้วยังมีเส้นสีต่าง ๆ ปรากฏในแถบสเปกตรัมด้วย และจากการสังเกตสเปกตรัม ของแก๊สไฮโดรเจน ฮีเลียม นีออน และไอปรอท พบว่าธาตุแต่ละชนิดให้สเปกตรัมที่มีเส้นสีต่างกันและมี จำ นวนเส้นสีเฉพาะตัว เส้นสีต่าง ๆ นี้เรียกว่า เส้นสเปกตรัม (spectrum line)

แถบสเปกตรัมของแสงขาวและเส้นสเปกตรัมของธาตุบางชนิด
ธาตุต่าง ๆ เมื่อได้รับพลังงานจะเปล่งแสงเป็นสีต่าง ๆ หลายสีเมื่อสีเหล่านั้นรวมกันแล้วจะ สังเกตเห็นเป็นสีเดียวซึ่งตาเราไม่สามารถบอกความแตกต่างได้ แต่เมื่อใช้แผ่นเกรตติงส่องดูจะเห็น เส้นสเปกตรัมของแต่ละธาตุที่มีลักษณะเฉพาะ เช่น จำ นวนเส้น สีหรือตำ แหน่งที่เกิดต่างกันไป การเกิด เส้นสเปกตรัมของธาตุอธิบายได้ว่า อิเล็กตรอนซึ่งเคลื่อนที่อยู่รอบนิวเคลียสมีพลังงานเฉพาะตัว ที่ต่ำ หรือกล่าวได้ว่าอะตอมอยู่ใน สถานะพื้น (ground state) เมื่ออะตอมได้รับพลังงานเพิ่มขึ้นทำ ให้ อิเล็กตรอนถูกกระตุ้นให้มีพลังงานสูงขึ้นหรือเรียกว่าอะตอมอยู่ใน สถานะกระตุ้น (excited state) ที่สถานะนี้อะตอมจะไม่เสถียร เนื่องจากมีพลังงานสูง อิเล็กตรอนจึงคายพลังงานออกมาส่วนหนึ่ง ทำ ให้อะตอมมีพลังงานลดลงแล้วกลับเข้าสู่สถานะที่มีพลังงานต่ำ ลงเพื่อให้อะตอมมีความเสถียร มากขึ้น พลังงานส่วนใหญ่ที่คายออกมาจะปรากฏในรูปพลังงานแสง และสามารถคำ นวณได้โดย ใช้ความสัมพันธ์ตามสมการของพลังค์ซึ่งได้กล่าวไว้แล้วในข้างต้น ถ้าแสงสีเหล่านี้แยกออกจากกัน อย่างชัดเจนจะปรากฏเป็นเส้นสเปกตรัม แต่ถ้าแสงสีที่ปรากฏออกมามีลักษณะต่อเนื่องกันเช่นเดียว กับรุ้งหรือจากไส้หลอดไฟฟ้าซึ่งเป็นโลหะร้อนและมีอะตอมอยู่กันอย่างหนาแน่น จะให้สเปกตรัมเป็น แถบสเปกตรัมซึ่งยากแก่การวิเคราะห์และแปลผล สภาวะของอิเล็กตรอนที่มีพลังงานต่าง ๆ เรียกว่า ระดับพลังงานของอิเล็กตรอน (energy level of electron)
จากการศึกษาเส้นสเปกตรัมของอะตอมไฮโดรเจนซึ่งมี1 อิเล็กตรอน พบว่ามีเส้นสเปกตรัม ปรากฏในช่วงคลื่นที่มองเห็นได้โดยมีความยาวคลื่น 410 434 486 และ 656 นาโนเมตร ตามลำ ดับ เมื่อคำ นวณผลต่างระหว่างพลังงานของเส้นสเปกตรัมที่อยู่ถัดกัน จะได้ข้อมูลดังตาราง 2.2

จากข้อมูลในตาราง 2.2 แสดงว่าอะตอมของไฮโดรเจนมีพลังงานหลายระดับโดยความแตกต่าง ระหว่างพลังงานแต่ละระดับที่อยู่ถัดไปมีค่าไม่เท่ากันและความแตกต่างของพลังงานมีค่าน้อยลงเมื่อ ระดับพลังงานสูงขึ้น การที่นักวิทยาศาสตร์ใช้อะตอมของไฮโดรเจนเป็นตัวอย่างในการแปลความหมายของเส้นสเปกตรัม เพราะอะตอมของไฮโดรเจนมีอิเล็กตรอนเดียว จากการทดลองหลายครั้งพบว่า อะตอมของไฮโดรเจนให้ เส้นสเปกตรัมได้หลายเส้นที่มีลักษณะเหมือนกันทุกครั้ง จึงสรุปได้ว่าอิเล็กตรอนในอะตอมของไฮโดรเจน ขึ้นไปอยู่ในสถานะกระตุ้นที่มีพลังงานแตกต่างกันได้หลายระดับ ค่าพลังงานของเส้นสเปกตรัมแสดงให้เห็น ถึงการเปลี่ยนระดับพลังงานของอิเล็กตรอนในอะตอมจากระดับพลังงานสูงมายังระดับพลังงานต่ำ ดังรูป 2.8

รูป 2.8 การเปลี่ยนระดับพลังงานของอิเล็กตรอนในอะตอมของไฮโดรเจน
การเปลี่ยนแปลงพลังงานของอิเล็กตรอนระหว่างสถานะกระตุ้นและสถานะพื้นสามารถ อุปมานได้กับการกลิ้งลงขั้นบันไดของลูกบอล ดังรูป 2.9
จากรูปจะเห็นว่าพลังงานศักย์ณ บันไดแต่ละขั้นมีค่าไม่เท่ากัน โดยลูกบอลที่อยู่บันไดขั้นต่ำจะมีพลังงานศักย์ต่ำ กว่าบันไดขั้นสูง และผลต่างของพลังงานระหว่างบันไดสองขั้นมีค่าเฉพาะตัว ที่แน่นอนโดยขั้นบันไดที่อยู่ห่างกันมากจะมีผลต่างของพลังงานมากกว่าขั้นบันไดที่อยู่ติดกัน เช่น ผลต่างของพลังงานระหว่างขั้นที่ 1 กับขั้นที่ 3 จะมีค่ามากกว่าขั้นที่ 1 กับขั้นที่ 2 หรืออาจสรุปได้ว่า ผลต่างของพลังงานศักย์ระหว่างขั้นบันไดขึ้นอยู่กับความแตกต่างระหว่างความสูงของขั้นบันไดและ มีค่าเฉพาะตัว การกลิ้งลงขั้นบันไดของลูกบอล ลูกจะต้องกลิ้งลงและหยุดที่ขั้นบันไดเท่านั้น ลูกบอล ไม่สามารถหยุดระหว่างขั้นบันไดได้เนื่องจากไม่มีที่พักระหว่างขั้นบันได ลูกบอลอาจกลิ้งและหยุดบน ขั้นบันไดขั้นที่ติดกันหรือขั้นที่อยู่ห่างออกไปได้เช่น จากขั้นที่ 5 ลงมายังขั้นที่ 4 หรือจากขั้นที่ 3 ลง มาขั้นที่ 1
จากการศึกษาเส้นสเปกตรัมของอะตอมไฮโดรเจนทำ ให้นักวิทยาศาสตร์สรุปได้ว่า 1. เมื่ออิเล็กตรอนได้รับพลังงานในปริมาณที่เหมาะสม อิเล็กตรอนจะขึ้นไปอยู่ในระดับพลังงาน ที่สูงกว่าระดับพลังงานเดิม แต่จะอยู่ในระดับใดขึ้นกับปริมาณพลังงานที่ได้รับ การที่อิเล็กตรอน ขึ้นไปอยู่ในระดับพลังงานใหม่ทำ ให้อะตอมไม่เสถียร อิเล็กตรอนจะกลับมาอยู่ในระดับพลังงานที่ต่ำ กว่า ซึ่งการเปลี่ยนตำ แหน่งของแต่ละระดับพลังงานนี้ อิเล็กตรอนจะคายพลังงานออกมาในรูปของ คลื่นแม่เหล็กไฟฟ้าด้วยความถี่เฉพาะค่าหนึ่งหรือกล่าวได้ว่าการดูดหรือคายพลังงานของอิเล็กตรอน ในอะตอมต้องมีค่าเฉพาะตามทฤษฎีของพลังค์โดยมีค่าเท่ากับความถี่ของคลื่นแม่เหล็กไฟฟ้านั้นคูณ ด้วยค่าคงที่ของพลังค์ดังที่กล่าวมาแล้ว 2. การเปลี่ยนระดับพลังงานของอิเล็กตรอนไม่จำ เป็นต้องเปลี่ยนไปยังระดับพลังงานที่อยู่ติดกัน อาจมีการเปลี่ยนข้ามระดับพลังงานได้และจะอยู่ระหว่างระดับพลังงานไม่ได้ 3. ผลต่างระหว่างพลังงานของระดับพลังงานต่ำ จะมีค่ามากกว่าผลต่างระหว่างพลังงานของ ระดับพลังงานที่สูงขึ้นไป จากความรู้เรื่องการเปลี่ยนแปลงระดับพลังงานของอิเล็กตรอนและการเกิดสเปกตรัม ช่วยให้ นีลส์ โบร์ (Niels Bohr) นักวิทยาศาสตร์ชาวเดนมาร์ก สร้างแบบจำ ลองอะตอมเพื่อใช้อธิบาย พฤติกรรมของอิเล็กตรอนในอะตอมได้ โดยกล่าวว่า อิเล็กตรอนจะเคลื่อนที่รอบนิวเคลียสเป็น วงคล้ายกับวงโคจรของดาวเคราะห์รอบดวงอาทิตย์ แต่ละวงจะมีระดับพลังงานเฉพาะตัว ระดับพลังงานของอิเล็กตรอนที่อยู่ใกล้นิวเคลียสที่สุดมีพลังงานต่ำ ที่สุดเรียกว่าระดับ K และระดับพลังงานที่อยู่ถัดออกมาเรียกเป็น L M N … ตามลำดับ ดังรูป 2.10
รูป 2.10 แบบจำลองอะตอมของโบร์ที่แสดงระดับพลังงานของอิเล็กตรอน
ต่อมาได้มีการใช้ตัวเลขแสดงถึงระดับพลังงานของอิเล็กตรอน คือ n = 1 หมายถึงระดับ พลังงานที่ 1 ซึ่งอยู่ ใกล้กับนิวเคลียสที่สุด และชั้นถัดออกมาเป็น n = 2 หมายถึงระดับพลังงานที่ 2 ต่อจากนั้น
n = 3 4 … หมายถึงระดับ พลังงานที่ 3 4 และสูงขึ้นไปตามลำดับ
2.1.5 แบบจำลองอะตอมแบบกลุ่มหมอก
แบบจำลองอะตอมของโบร์มีข้อจำกัดคือไม่สามารถใช้อธิบายสเปกตรัมของอะตอมที่มีหลาย อิเล็กตรอนได้นักวิทยาศาสตร์จึงได้ศึกษาเพิ่มเติมจนได้ข้อมูลเพียงพอที่จะเชื่อว่าอิเล็กตรอนมีสมบัติ เป็นทั้งอนุภาคและคลื่นโดยเคลื่อนที่รอบนิวเคลียส บริเวณที่พบอิเล็กตรอนมีหลายลักษณะเป็นรูปทรง ต่าง ๆ ตามระดับพลังงานของอิเล็กตรอน จากการประยุกต์ใช้สมการทางคณิตศาสตร์และใช้คอมพิวเตอร์ ช่วยในการคำ นวณ เพื่อหาโอกาสที่จะพบอิเล็กตรอนในระดับพลังงานต่าง ๆ พบว่าสามารถอธิบาย เส้นสเปกตรัมของธาตุได้ถูกต้องกว่าแบบจำลองอะตอมของโบร์และสามารถอธิบายได้ว่าอิเล็กตรอน มีขนาดเล็กมากและเคลื่อนที่อย่างรวดเร็วตลอดเวลาไปทั่วทั้งอะตอม จึงไม่สามารถบอกตำแหน่งที่แน่นอน ของอิเล็กตรอนได้ อย่างไรก็ตามนักวิทยาศาสตร์พบว่ามีโอกาสที่จะพบอิเล็กตรอนรอบนิวเคลียส บางบริเวณเท่านั้น ทำ ให้สร้างมโนภาพได้ว่าอะตอมประกอบด้วยกลุ่มหมอกอิเล็กตรอน (electron cloud) รอบนิวเคลียส บริเวณที่กลุ่มหมอกทึบแสดงว่ามีโอกาสที่จะพบอิเล็กตรอนได้มากกว่าบริเวณ ที่มีกลุ่มหมอกจาง เรียกแบบจำลองนี้ว่าแบบจำลองอะตอมแบบกลุ่มหมอก (electron cloud model of atom) ดังรูป 2.11 (แต่ละจุดคือ 1 โอกาสที่จะพบอิเล็กตรอน)
รูป 2.11 ภาพ 2 มิติแสดงกลุ่มหมอกอิเล็กตรอนของไฮโดรเจนอะตอมซึ่งมี 1 อิเล็กตรอน
แบบจำลองอะตอมแบบกลุ่มหมอกที่แสดงถึงความหนาแน่นของอิเล็กตรอนรอบนิวเคลียส ทำได้ยาก โดยทั่วไปจึงพิจารณาอะตอมในลักษณะทรงกลม เช่น ลูกปิงปอง หรือพลาสติกทรงกลม เป็นแบบจำลองแทนอะตอมของธาตุ แต่นักเรียนควรระลึกไว้เสมอว่าการใช้แบบจำ ลองเช่นนี้เพียง เพื่อช่วยให้คิดตามได้ง่ายขึ้นเท่านั้น เมื่อนักเรียนได้ศึกษาในระดับที่สูงขึ้นไปจะพบว่ารูปทรงของกลุ่ม หมอกอิเล็กตรอนไม่ได้มีเพียงรูปทรงกลมเท่านั้น โครงสร้างอะตอมตามแบบจำลองอะตอมแบบกลุ่มหมอกยังไม่ใช่ข้อยุติในการศึกษาทดลองเกี่ยวกับอะตอม เพราะความรู้ทางวิทยาศาสตร์มีการพัฒนาอย่างต่อเนื่องตลอดเวลา ดังนั้นในอนาคตจึงอาจมีแบบจำลองอะตอมแบบอื่นตามข้อมูลที่ค้นพบใหม่
2.2 อนุภาคในอะตอมและไอโซโทป
ในหัวข้อที่ผ่านมานักเรียนได้ทราบแล้วว่าทอมสันค้นพบอิเล็กตรอนและค่าประจุต่อมวล ในหัวข้อนี้นักเรียนจะได้เรียนรู้เกี่ยวกับอนุภาคชนิดอื่นที่เป็นองค์ประกอบของอะตอม
2.2.1 อนุภาคในอะตอม
ในปีพ.ศ. 2451 รอเบิร์ต แอนดรูส์มิลลิแกน (Robert Andrews Millikan) นักวิทยาศาสตร์ ชาวอเมริกันได้ทำ การหาค่าประจุของอิเล็กตรอนโดยอาศัยการสังเกตหยดน้ำ มันในสนามไฟฟ้า ดังรูป 2.12
รูป 2.12 การทดลองหยดน้ำมันมิลลิแกน
เมื่อละอองน้ำมันที่ร่วงผ่านรูบนขั้วไฟฟ้าบวกกระทบรังสีจะมีประจุไฟฟ้าเกิดขึ้น ทำให้ละออง น้ำมันบางหยดเคลื่อนที่เข้าหาขั้วไฟฟ้าบวก บางหยดเข้าหาขั้วไฟฟ้าลบ และบางหยดลอยนิ่งอยู่ระหว่าง สนามไฟฟ้า ขนาดของหยดน้ำมันที่ลอยนิ่งอยู่ระหว่างสนามไฟฟ้าสามารถสังเกตได้จากกล้องจุลทรรศน์ และนำมาคำนวณหามวลของหยดน้ำมันที่ทราบความหนาแน่นของน้ำมัน และจากความสัมพันธ์ของน้ำหนักของหยดน้ำมันที่ลอยนิ่งเท่ากับแรงที่เกิดจากสนามไฟฟ้า ทำให้สามารถคำ นวณค่าประจุไฟฟ้าบนหยดน้ำมันได้ซึ่งพบว่าประจุไฟฟ้าบนหยดน้ำมันมีค่าเป็นจำนวนเท่าของ 1.60 × 10^-19 คูลอมบ์ มิลลิแกนจึงสรุปว่าประจุของอิเล็กตรอนมีค่าเท่ากับ 1.60 × 10^-19 คูลอมบ์เมื่อนำ มาใช้คำนวณร่วมกับค่าประจุต่อมวลที่รายงานไว้โดยทอมสันจะได้มวลของอิเล็กตรอนเท่ากับ 9.11 × 10^-28 กรัม
ในปีพ.ศ. 2429 ออยเกน โกลด์ชไตน์(Eugen Goldstein) ได้ทำ การดัดแปลงหลอดรังสีแคโทด โดยการสลับตำแหน่งของแคโทดและแอโนด ดังรูป 2.13 ซึ่งเมื่อผ่านกระแสไฟฟ้าเข้าไปพบว่า ฉาก เกิดการเรืองแสง แสดงว่ามีรังสีออกจากแอโนด ซึ่งโกลด์ชไตน์เรียกรังสีชนิดนี้ว่า รังสีแคแนล (canal ray) หรือรังสีแอโนด (anode ray) ซึ่งมีประจุบวก
รูป 2.13 หลอดรังสีแคโทดที่ดัดแปลง
โกลด์ชไตน์ได้ทำ การทดลองกับแก๊สหลายชนิดพบว่ารังสีแอโนดมีค่าประจุต่อมวล (e/m) ไม่คงที่ จนกระทั่งกลุ่มนักวิจัยนำ ทีมโดยรัทเทอร์ฟอร์ดและทอมสัน ได้ทำ การศึกษาหลอดในลักษณะเดียวกัน ที่บรรจุแก๊สไฮโดรเจน ทำ ให้ได้ข้อสรุปว่าอนุภาคบวกมีค่าประจุเท่ากันกับอิเล็กตรอน และหาค่ามวล ของประจุบวกได้เป็น 1.673 × 10^-24 กรัม ซึ่งมากกว่ามวลของอิเล็กตรอนประมาณ 1,840 เท่า เรียก อนุภาคนี้ว่า โปรตอน (proton)
ในปีพ.ศ. 2475 เจมส์แชดวิก (James Chadwick) นักวิทยาศาสตร์ชาวอังกฤษได้ทดลองยิง อนุภาคแอลฟาไปยังอะตอมของธาตุต่าง ๆ และทดสอบผลการทดลองด้วยเครื่องมือที่มีความเที่ยงสูง ทำ ให้ทราบว่าในนิวเคลียสมีอนุภาคที่เป็นกลางทางไฟฟ้าและเรียกอนุภาคนี้ว่า นิวตรอน (neutron) ซึ่งมีมวลใกล้เคียงกับมวลของโปรตอน การค้นพบนิวตรอนช่วยอธิบายและสนับสนุนข้อมูลเกี่ยวกับ มวลของอะตอม ซึ่งพบว่ามีค่ามากกว่ามวลรวมของโปรตอน เช่น ธาตุคาร์บอนมีมวลของโปรตอน รวมกัน 6 หน่วย แต่มวลของอะตอมมีค่า 12 หน่วย และมวลของธาตุส่วนใหญ่มีค่าเป็น 2 เท่าหรือ มากกว่า 2 เท่าของมวลโปรตอนทั้งหมดรวมกัน ดังนั้น อิเล็กตรอน โปรตอน และนิวตรอน จึงเป็น อนุภาคในอะตอม (subatomic particle) ซึ่งอนุภาคแต่ละชนิดมีรายละเอียดดังตาราง 2.3
2.2.2 เลขอะตอม เลขมวล และไอโซโทป อะตอมประกอบด้วยโปรตอนและนิวตรอนรวมกันเป็นนิวเคลียสของอะตอม และมีอิเล็กตรอน ซึ่งมีจำ นวนเท่ากับจำ นวนโปรตอนเคลื่อนที่อยู่รอบนิวเคลียส อะตอมของธาตุแต่ละชนิดมีจำ นวน โปรตอนเฉพาะตัวไม่ซ้ำ กับธาตุอื่น ตัวเลขที่แสดงจำ นวนโปรตอนเรียกว่า เลขอะตอม (atomic number, Z) และเนื่องจากมวลของอิเล็กตรอนมีค่าน้อยมาก ดังนั้นมวลของอะตอมส่วนใหญ่จึงเป็น มวลของนิวเคลียสที่ประกอบด้วยโปรตอนและนิวตรอน เรียกผลรวมของจำ นวนโปรตอนและ นิวตรอนว่า เลขมวล (mass Number, A) เช่น คาร์บอนมี6 โปรตอนจึงมีเลขอะตอมเท่ากับ 6 โดย อาจมี 6 หรือ 7 นิวตรอน จึงมีเลขมวลเป็น 12 หรือ 13 ตามลำดับ สัญลักษณ์ที่เขียนแสดงรายละเอียดเกี่ยวกับสัญลักษณ์ของธาตุเลขอะตอม และเลขมวลของ อะตอม เรียกว่า สัญลักษณ์นิวเคลียร์ (nuclear symbol) วิธีเขียนที่ตกลงกันเป็นสากล ให้เขียน เลขอะตอมไว้ด้านล่างซ้าย และเลขมวลไว้ด้านบนซ้ายของสัญลักษณ์ดังรูป 2.14
รูป 2.14 สัญลักษณ์นิวเคลียร์
อะตอมของธาตุชนิดเดียวกันมีจำ นวนโปรตอนและอิเล็กตรอนเท่ากัน แต่จำ นวนนิวตรอน อาจมีได้หลายค่า ทำ ให้อะตอมของธาตุเดียวกันมีมวลต่างกัน เฟรเดอริก ซอดดี(Frederick Soddy) นักเคมีชาวอังกฤษ เรียกอะตอมของธาตุเดียวกันที่มีเลขมวลต่างกันว่า ไอโซโทป (isotope) ธาตุชนิด หนึ่งอาจมีหลายไอโซโทป บางไอโซโทปมีอยู่ในธรรมชาติและบางไอโซโทปได้จากการสังเคราะห์เช่น ไฮโดรเจน มี3 ไอโซโทป มีเลขมวล 1 2 และ 3 มีชื่อเฉพาะว่า โปรเทียม (protium) ดิวทีเรียม (deuterium) และ ทริเทียม (tritium) ตามลำ ดับ ไฮโดรเจนที่เกิดในธรรมชาติมีปริมาณโปรเทียมอยู่ถึง ร้อยละ 99.99 แต่ละไอโซโทปของไฮโดรเจนเขียนสัญลักษณ์นิวเคลียร์ได้เป็น ₁¹H ₁²H และ ₁³H อาจเขียนอย่างย่อโดยเขียนเฉพาะสัญลักษณ์ของธาตุกับเลขมวลก็ได้โดยเขียนเป็น ¹H ²H และ ³H หรือ H-1 H-2 และ H-3 แต่ละไอโซโทปของไฮโดรเจนมีชื่อเฉพาะ และใช้สัญลักษณ์แทนดังตาราง 2.4
คาร์บอนมีเลขอะตอม 6 มี3 ไอโซโทป ซึ่งมีเลขมวล 12 13 และ 14 สัญลักษณ์นิวเคลียร์ จึงเป็น
¹²₆C ¹³₆C และ ¹⁴₆C เขียนแบบย่อเป็น ¹²C ¹³C และ ¹⁴C หรือ C-12 C-13 และ C-14 การเรียก ชื่อของไอโซโทปของธาตุจะเรียกขึ้นต้นด้วยชื่อของธาตุและตามด้วยเลขมวล เช่น ¹⁴C มีเลขมวล 14 จะมี6 โปรตอน และ 8 นิวตรอน เรียกไอโซโทปนี้ว่า คาร์บอน-14 (C-14)
2.3 การจัดเรียงอิเล็กตรอนในอะตอม
2.3.1 จำนวนอิเล็กตรอนในแต่ละระดับพลังงาน
จากการศึกษาแบบจำลองอะตอม ทำให้ทราบว่าอะตอมประกอบด้วยโปรตอนและนิวตรอน อยู่รวมกันในนิวเคลียส โดยมีอิเล็กตรอนเคลื่อนที่อยู่รอบ ๆ และอยู่ในระดับพลังงานต่างกัน อิเล็กตรอน เหล่านั้นอยู่กันอย่างไรและในแต่ละระดับพลังงานจะมีจำ นวนอิเล็กตรอนสูงสุดเท่าใด ให้นักเรียน พิจารณาข้อมูลแสดงการจัดเรียงอิเล็กตรอนของธาตุบางธาตุดังตาราง 2.5
เมื่อพิจารณาข้อมูลในตาราง 2.5 จะพบว่าจำ นวนอิเล็กตรอนในระดับพลังงานที่ 1 มีได้มาก ที่สุด 2 อิเล็กตรอน ระดับพลังงานที่ 2 มีได้มากที่สุด 8 อิเล็กตรอน สำ หรับระดับพลังงานที่ 3 นั้น จากการสืบค้นข้อมูลเพิ่มเติมทำ ให้ทราบว่ามีได้มากที่สุด 18 อิเล็กตรอน นั่นคือ จำนวนอิเล็กตรอน มากที่สุดที่มีได้ในแต่ละระดับพลังงานจะมีค่าเท่ากับ 2n² เมื่อ n คือ ตัวเลขแสดงระดับพลังงาน
ถ้าพิจารณาตามหลัก 2n² การจัดเรียงอิเล็กตรอนของธาตุ K และ Ca ควรเป็น 2 8 9 และ 2 8 10 ตามลำ ดับ เนื่องจากในระดับพลังงานที่ 3 ควรมีอิเล็กตรอนได้สูงสุดถึง 18 อิเล็กตรอน แต่ จากการศึกษาพบว่าการจัดเรียงอิเล็กตรอนของธาตุ K และ Ca เป็น 2 8 8 1 และ 2 8 8 2 ตาม ลำ ดับ ซึ่งหมายความว่าอิเล็กตรอนในระดับพลังงานที่ 3 ของทั้งสองธาตุนี้มีเพียง 8 อิเล็กตรอน และ อิเล็กตรอนที่เพิ่มมาอีก 1 และ 2 อิเล็กตรอนนั้นเข้าไปอยู่ในระดับพลังงานที่ 4 ทำ ให้ระดับพลังงานที่ 3 มีอิเล็กตรอนไม่ครบ 18 ข้อมูลดังกล่าวนี้จะได้ศึกษาต่อไป
2.3.2 ระดับพลังงานหลัก และระดับพลังงานย่อย
นักเรียนทราบมาแล้วว่าโบร์เสนอแบบจำลองโดยใช้ข้อมูลเกี่ยวกับเส้นสเปกตรัมของ ไฮโดรเจนซึ่งแสดงให้เห็นว่าอะตอมของไฮโดรเจนมีพลังงานหลายระดับและความแตกต่างระหว่าง พลังงานของแต่ละระดับที่อยู่ถัดไปก็ไม่เท่ากัน โดยความแตกต่างของพลังงานจะมีค่าน้อยลง เมื่อมีระดับพลังงานสูงขึ้น
การอธิบายเกี่ยวกับเส้นสเปกตรัมของโบร์ได้จุดประกายให้นักวิทยาศาสตร์หลายคนเกิดความ สนใจและศึกษาเกี่ยวกับเส้นสเปกตรัมมากขึ้น และพบว่าเส้นสเปกตรัมของไฮโดรเจนที่เปล่งแสง ออกมาและมองเห็นเป็น 1 เส้นนั้นแท้จริงแล้วประกอบด้วยเส้นสเปกตรัมมากกว่า 1 เส้น ซึ่งนำ ไปสู่ข้อสรุปที่ว่า เส้นสเปกตรัมที่เกิดขึ้น นอกจากเป็นการคายพลังงานของอิเล็กตรอนจากระดับพลังงานหลัก (principle energy level หรือ shell) ซึ่งแทนด้วย n แล้ว ยังเป็นการคายพลังงานของอิเล็กตรอนจาก ระดับพลังงานย่อย (energy sublevel หรือ subshell) ของแต่ละระดับพลังงานหลักอีกด้วย
นักวิทยาศาสตร์ได้กำ หนดระดับพลังงานย่อยเป็นตัวอักษร s p d และ f ตามลำ ดับ แนวคิด ดังกล่าวนี้สามารถนำ มาอธิบายสเปกตรัมของธาตุที่มีมากกว่า 1 อิเล็กตรอนได้ และจากการศึกษา เพิ่มเติมพบว่าจำ นวนระดับพลังงานย่อยที่เป็นไปได้ในแต่ละระดับพลังงานหลักที่ 1 – 4 เป็นดังนี้
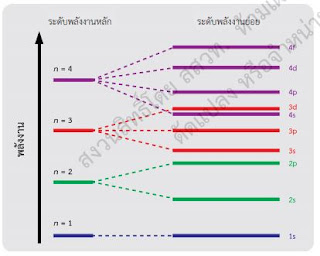
แผนภาพระดับพลังงานของอะตอมที่มีหลายอิเล็กตรอน
จากรูป 2.15 สามารถสรุปได้ว่า
ระดับพลังงานหลักที่ 1 (n = 1) มี1 ระดับพลังงานย่อยคือ s
ระดับพลังงานหลักที่ 2 (n = 2) มี2 ระดับพลังงานย่อยคือ s p
ระดับพลังงานหลักที่ 3 (n = 3) มี3 ระดับพลังงานย่อยคือ s p d ระดับพลังงานหลักที่ 4 (n = 4) มี4 ระดับพลังงานย่อยคือ s p d f
2.3.3 ออร์บิทัล
เนื่องจากอิเล็กตรอนมีการเคลื่อนที่ตลอดเวลา ความหนาแน่นของกลุ่มหมอกอิเล็กตรอนจึงอยู่ ในรูปของโอกาสที่จะพบอิเล็กตรอนซึ่งมีอาณาเขตและรูปร่างใน 3 มิติแตกต่างกัน บริเวณรอบนิวเคลียส ซึ่งมีโอกาสที่จะพบอิเล็กตรอนและมีพลังงานเฉพาะนี้เรียกว่าออร์บิทัล (orbital) จากศึกษาพบว่าจำ นวน ออร์บิทัลในแต่ละระดับพลังงานย่อยมีค่าแตกต่างกันซึ่งสามารถสรุปได้ดังนี้
ระดับพลังงานย่อย s มี 1 ออร์บิทัล
ระดับพลังงานย่อย p มี 3 ออร์บิทัล
ระดับพลังงานย่อย d มี 5 ออร์บิทัล
ระดับพลังงานย่อย f มี 7 ออร์บิทัล
จากรูป 2.15 ถ้าเขียนเป็นแผนผังโดยพิจารณาออร์บิทัลของแต่ละระดับพลังงานย่อยอาจเขียน แสดงได้ดังรูป 2.16
จำนวนอิเล็กตรอนสูงสุดในออร์บิทัลที่อยู่ในระดับพลังงานย่อย s p d และ f สามารถพิจารณาจากข้อมูลในตาราง 2.6

จากตาราง 2.6 จะเห็นว่าจำ นวนอิเล็กตรอนสูงสุดในระดับพลังงานย่อย s p d และ f มีค่าเท่ากับ 2 6 10 และ 14 ตามลำ ดับ แต่เนื่องจากพลังงานย่อย s p d และ f มี1 3 5 และ 7 ออร์บิทัลตามลำ ดับ แสดงว่า 1 ออร์บิทัลสามารถบรรจุอิเล็กตรอนได้ 2 อิเล็กตรอน
2.3.4 หลักการจัดเรียงอิเล็กตรอนในอะตอม
การจัดเรียงอิเล็กตรอนของอะตอมหนึ่ง ๆ ให้พิจารณาตาม หลักอาฟบาว (Aufbau principle) ซึ่งเกี่ยวข้องกับลำ ดับพลังงานของแต่ละออร์บิทัล กล่าวคือการบรรจุอิเล็กตรอนต้องบรรจุในออร์บิทัล ที่มีพลังงานต่ำ สุดและว่างอยู่ก่อนเสมอ ดังรูป 2.17 นั่นคือเริ่มจาก 1s 2s 2p 3s … ตามลำ ดับ เพราะจะทำ ให้พลังงานรวมทั้งหมดมีค่าต่ำ ที่สุดและอะตอมมีความเสถียรที่สุด
รูป 2.17 แผนภาพแสดงลำดับการบรรจุอิเล็กตรอนในออร์บิทัลต่าง ๆ
จากแผนภาพสามารถเรียงลำ ดับพลังงานได้ดังนี้ 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p …
ไฮโดรเจนอะตอมซึ่งมี1 อิเล็กตรอน สามารถเขียนสัญลักษณ์แสดงการจัดเรียงอิเล็กตรอนได้ เป็น 1s¹ โดยมีความหมายดังนี้
รูป 2.18 สัญลักษณ์แสดงการจัดเรียงอิเล็กตรอนของไฮโดรเจนอะตอม






























ไม่มีความคิดเห็น:
แสดงความคิดเห็น